Apa itu...Termodinamika
Termodinamika berarti ilmu yang membahas tentang suhu,kalor,dan usaha mekanik pada gas (sistem).
Sistem berarti sejumlah gas yang terdapat dalam wadah tertutup.
Kalau kita panaskan gas yang ada ditabung, gas pasti memuai, maka piston bergerak keatas.
Diagram p - V
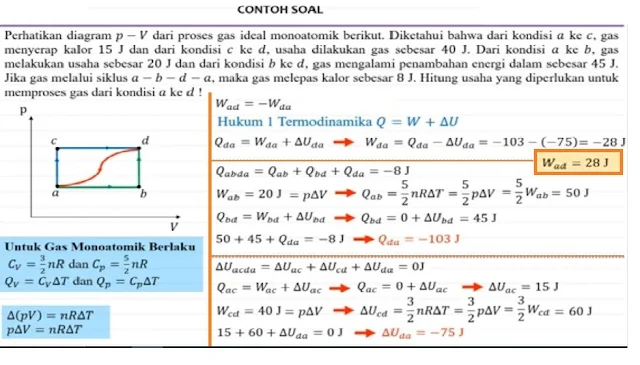
Kalau p dan V diketahui, usaha yang dikerjakan sistem atau gas,sama dengan luas di bawah kurva pV.
Catatan :
Siapakah ahli fisika yang mendalami teori termodinamika?
Banyak ahli fisika yang telah mendalami teori termodinamika, dan beberapa di antaranya dianggap sebagai tokoh kunci dalam pengembangan teori ini. Beberapa fisikawan terkemuka yang telah memberikan kontribusi besar dalam bidang termodinamika antara lain:
1. Sadi Carnot: Merupakan tokoh awal dalam pengembangan teori termodinamika. Ia dikenal karena konsep mesin Carnot, yang menjadi dasar untuk pemahaman termodinamika siklus.
2. Rudolf Clausius: Menyumbangkan ide mengenai konsep entropi dan merumuskan pernyataan kedua hukum termodinamika.
3. Lord Kelvin (William Thomson): Berkontribusi pada formulasi hukum termodinamika kedua dan mengembangkan konsep termodinamika mutlak.
4. James Clerk Maxwell: Mengintegrasikan teori kinetika gas dengan termodinamika dan merumuskan distribusi Maxwell-Boltzmann.
5. Ludwig Boltzmann: Merupakan salah satu pemikir utama dalam memahami interpretasi statistik termodinamika dan memberikan kontribusi pada pengembangan mekanika statistik.
6. Josiah Willard Gibbs: Merumuskan teori termodinamika secara matematis, termasuk konsep energi bebas dan potensial kimia. Ia juga memperkenalkan istilah "entropi."
7. Albert Einstein: Memberikan kontribusi pada pemahaman pergerakan Brownian dan konsep panas jenis partikel (foton). Teori khusus relativitasnya juga memiliki dampak pada termodinamika.
8. Enrico Fermi: Berkontribusi pada pemahaman perilaku gas pada suhu rendah dan mendalami konsep statistik dalam termodinamika.
Tentu saja, masih banyak fisikawan lainnya yang juga memberikan kontribusi besar dalam pengembangan teori termodinamika. Keberhasilan teori ini banyak bergantung pada kerja kolaboratif dan perkembangan sepanjang waktu.
CONTOH LAIN :
Contoh lain :
1. Ketika usaha 2,00 x 103 J diberikan secara adiabatik untuk memampatkan setengah mol suatu gas ideal monoatomik, suhu mutlaknya menjadi dua kali semula. Tentukan suhu awal gas. R = 8,31 J/(mol K).
Gunakan persamaan hukum I Termodinamika
2. Gas monoatomik sebanyak 2 mol mula mula bersuhu 27°C dan tekanannya 3×105 Pa mengalami proses isokhorik sehingga tekanan nya menjadi 4×105 Pa. Besar perubahan energi dalam gas bila terapan gas universal 8,31 J/mol K adalah..?












Tidak ada komentar:
Posting Komentar